Struttura delle proteine
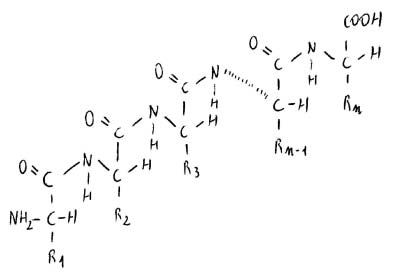
Polimero peptidico vettoriale: i due amminoacidi terminali non sono equivalenti (αC ha NH2, αCn ha NH; 1C1 ha NH, 1Cn ha OH).
TERMINALE 1: N-terminale
TERMINALE n: C-terminale
Il legame C-N è diverso dagli altri legami carbonilici conosciuti.
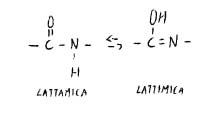
Nel caso di un peptide l’equilibrio è spostato verso destra (confermato da misure di lunghezza di legame): corrisponde ad un doppio legame; ciò vuol dire che si ha una certa rigidità e che si ha stereoisomeria geometrica.
È positivo alla reazione del biureto.
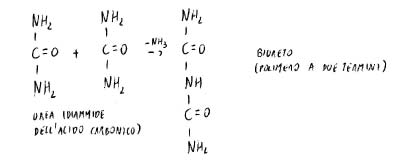
N-H blocca la possibile risonanza del legame del biureto. Aumenta quindi esponenzialmente la frequenza di risonanza del doppio legame sulle posizioni terminali (opposizione alla risonanza).
In soluzione l’equilibrio è spostato verso il biureto; in presenza di Cu2+ si forma un complesso.
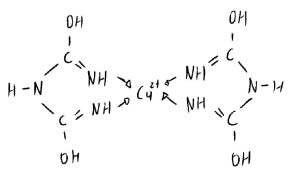
Il peptide presenta forma lattimica e può complessare Cu2+ (reazione qualitativa e quantitativa).
Analisi sequenziale
In condizioni anidre.
Si utilizza il feniltioisocianato che reagisce con l’azoto di αC, quindi in un peptide reagisce solo quello in posizione 1.
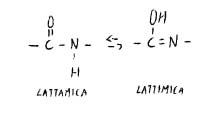
Nel caso di un peptide l’equilibrio è spostato verso destra (confermato da misure di lunghezza di legame): corrisponde ad un doppio legame; ciò vuol dire che si ha una certa rigidità e che si ha stereoisomeria geometrica.
È positivo alla reazione del biureto.

N-H blocca la possibile risonanza del legame del biureto. Aumenta quindi esponenzialmente la frequenza di risonanza del doppio legame sulle posizioni terminali (opposizione alla risonanza).
In soluzione l’equilibrio è spostato verso il biureto; in presenza di Cu2+ si forma un complesso.

Il peptide presenta forma lattimica e può complessare Cu2+ (reazione qualitativa e quantitativa).
Analisi sequenziale
In condizioni anidre.
Si utilizza il feniltioisocianato che reagisce con l’azoto di αC, quindi in un peptide reagisce solo quello in posizione 1.
Continua a leggere:
- Successivo: Degradazione di Edman
- Precedente: PROTEINE
Puoi scaricare gratuitamente questo appunto in versione integrale.

