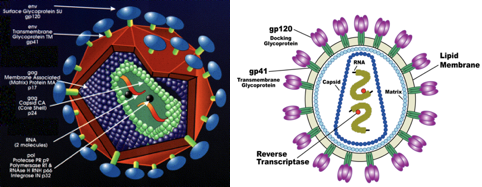
La principale cellula ospite è rappresentata dai linfociti T che esprimono nella loro superficie una molecola di CD4.
Replicazione del virus dell'HIV
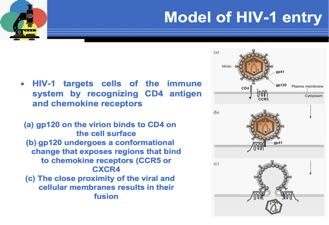
Nella diapositiva si illustra i meccanismi che il virus mette in atto per infettare la cellula ospite. La prima proteina che partecipa è la proteina più superficiale presente nell’envelope che è la Gp120. Questa interagisce con la molecola Cd4 presente nella cellula bersaglio e questo legame comporta un cambio conformazionale della Gp120; non si accontenta l'HIV di un solo recettore, ha bisogno di contrarre con la cellula ospite anche un secondo legame che è mediato dal legame della Gp120 con un corecettore C, il quale è rappresentato da una molecola di CCR5. Quindi un primo legame Gp120 e Cd4 cambio conformazionale a livello della Gp 120 legame della Gp 120 con un corecettore che nel nostro esempio era rappresentato da una molecola di CCR5.
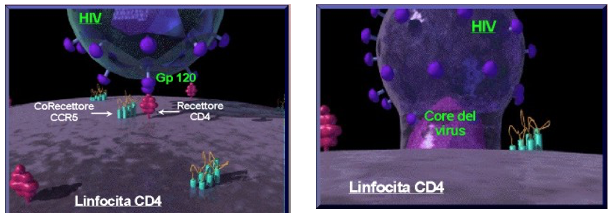
Il legame al Cd4 e al corecettore determina un ulteriore cambio di conformazione che espone la Gp41.
In questa diapositiva è rappresentato da un cono scuro e così esposta la molecola di Gp41 fonde l' envelope virale con la membrana citoplasmatica della cellula ospite.
Questo corecettore CCR5 è presente sui macrofagi mentre un altro corecettore CXCR4 è il corecettore localizzato sui linfociti, quindi avremo tropismo dell'HIV nel primo caso che riguardi il macrofago mentre nel secondo caso nei riguardi dei linfociti CB4P1. Quando è avvenuto il legame recettore-corecettore la membrana citoplasmatica della cellula e l'envelope virale sono ravvicinati, si espone la glicoproteina 41 ed ecco qui la fusione con l'ingresso del CORE virale nel citoplasma della cellula ospite. Il passaggio successivo è quello del primo complesso chiamato complesso della trascrittasi inversa.
Questa diapositiva è un passo indietro che ci mostra come il tropismo del HIV nei riguardi dei linfociti è determinato dal fatto che la CXCR4 il corecettore è presente nei linfociti mentre nei macrofagi il corecettore è rappresentato da una molecola di CCR5.
Cosa sono questi CXCR4 e CCR5? Che ruolo fisiologico hanno?
Sono importanti proteine segnali che svolgono la loro funzione nel corso della risposta immunitaria. Eravamo arrivati alla liberazione del core nel citoplasma, una volta che è il core si è liberato nel citoplasma inizia il processo di trascrittasi inversa. Nel complesso della trascrittasi inversa abbiamo le due coppie di RNA genomico, i transfer della Lisina (la trascrittasi inversa ha bisogno di un innesco rappresentato da una molecola di transfer che si porta dietro dalla cellula nella quale si è formato) inoltre troviamo l'integrasi, la proteina matrice,la nucleoproteina,la proteina Vpr come pure si complessano a questo complesso diverse proteine cellulari. Questo è un momento critico fondamentale della replicazione dell'HIV in cui il genoma, RNA lineare monocatenario, viene convertito in un DNA bicatenario e va a infiltrarsi nel cromosoma della cellula ospite. Si forma il complesso di pre-integrazione.
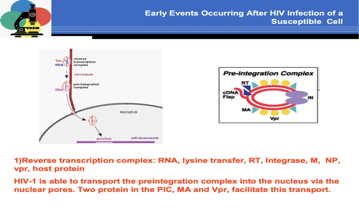
L'RNA viene convertito in DNA bicatenario e con l'intervento della matrice di Vpr questo complesso riesce a passare nel nucleo attraverso i pori nucleari. Questo è molto importante perché molti retrovirus non hanno questa possibilità, infatti per entrare in sede nucleare hanno bisogno che la cellula si divida e quando viene a mancare l'integrità della membrana cellulare possono entrare. Diversamente solo l'HIV riesce a passare attraverso i pori nucleari e questo ci dice che il virus riesce ad entrare anche in cellule quiescenti.
Cosa succede una volta che il complesso pre-integrazione entra nel nucleo? Grazie all'intervento della integrasi il pro virus viene può essere integrato nel cromosoma della cellula ospite.
Slide schematizzate le tappe della trascrittasi inversa: Vediamo come la prima funzione della trascrittasi inversa è quella di comportarsi come una Dna polimerasi RNA indipendente, lo stampo di RNA genomico colorato in giallo sintetizza una prima catena di DNA che sarà il DNA a polarità negativa, dopo di che scatta la seconda funzione enzimatica della trascrittasi inversa, l'RNAasi H che digerisce l'RNA e infine grazie alla capacità di funzionare come un una DNA polimerasi DNA dipendente arriviamo alla fine che tutta la informazione genetica originariamente contenuta in una molecola di RNA è ora contenuta in un DNA bicatenario provirus che andrà ad integrarsi nella cellula ospite. È importante ancora una volta sottolineare che la trascrittasi inversa funziona in modo estremamente inaccurato introducendo ogni volta che copia un genoma da 1 a 10 mutazioni. Ecco che si viene a creare un popolazione caratterizzata da una varietà enorme per la quale è stato coniato il termine di “quasi Specie”. La trascrittasi inversa compie dei salti, e il risultato di questo saltare dall'estremià 5'all'estremità 3'è che alla fine di questo processo, parliamo di quando sono state sintetizzate due catene di DNA tra loro complementari, si sono formate in seguito a questi salti sia all'estremità 5'che a quella 3'del provirus delle sequenze chiamate LTR, ciascuna caratterizzata dalla presenza della sequenza U3, R e U5. Sono queste le zone, in particolare U3 dove si legheranno i fattori di trascrizione che regoleranno e determineranno la possibilità del virus di esprimersi. Esprimersi vuol dire che la sequenza U3 localizzata in posizione 5'fisserà fattori di trascrizione che consentiranno alla RNA polimerasi 2 della cellula di sintetizzare messaggeri virus specifici. L'RNA inizialmente è caratterizzato da una sequenza unica all'estremità 5'e da una sequenza unica U3 all'estremità 3'. Ad entrambe le estremità sono presenti delle sequenze direttamente ripetute che nello schema sono quelle indicate con R. Le regioni U3, R e U5 sono importanti nella regolazione dell'espressione del HIV una volta che è stato integrato. Vediamo il funzionamento della integrasi: in punti casuali l integrasi è in grado di tagliare il cromosoma dell'ospite e inserire il pro virus, questo pro virus integrato sarà riconosciuto purché siano presenti dei particolari fattori che attivano la trascrizione dall'RNA polimerasi cellulare e avremo così la possibilità che si mettano a sintetizzare gli RNA messaggeri e virali.
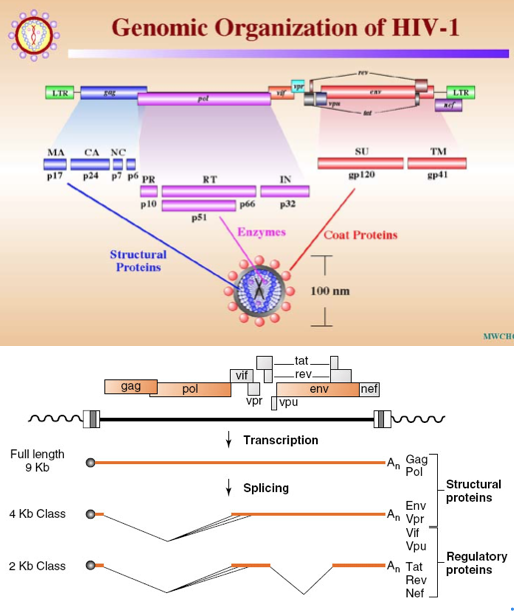
Rispetto al genoma dei retrovirus l'organizzazione genomica del HIV è ben più complessa.
Qui vediamo un pro virus integrato con le LTR ad entrambe le estremità e seguono poi tre geni presenti in tutti i retrovirus: GAG POL ENV. GAG informazione genetica per la sintesi delle proteine strutturali interne del virus: proteina di matrice, proteina capsidica P24 e la proteina nucleocapsidica che avvolge il genoma ad RNA. POL ha l informazione genetica che porta alla sintesi delle tre attività enzimatiche proteasi, trascrittasi inversa e integrasi. ENV porta invece l'informazione per la sintesi delle 2 glicoproteine Gp120 e GP41 che troviamo nell'envelope virale.
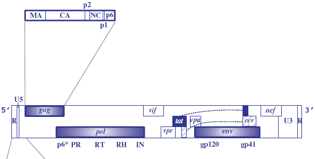
Questi sono i tre Geni che caratterizzano tutti i retro virus e sono sufficienti per il processo di replicazione del virus.
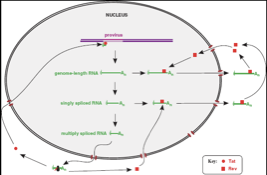
In aggiunta HIV possiede altri 6 geni che hanno funzione regolatoria o accessoria, tra questi importanti sono il gene TAT e REV.
REV consentirà di esportare i messaggeri cellulari non sottoposti a splicing o sottoposti ad un solo processo di splicing dal nucleo al citoplasma (omologo di REX).
L'altro gene è TAT e grazie a questo si possono formare i messaggeri virali completi.
In assenza di TAT il processo di trascrizione sui provirus integrati si arresta molto precocemente.
Poi abbiamo un'altra serie di geni: vif, vpu, nef, manca il sesto gene in questa tabella di questi geni regolatori accessori il quale è rappresentato dal gene vpr. Come vanno le cose? allora partiamo dal momento in cui utilizzando come stampo il pro virus integrato l RNA polimerasi trascrive formando i messaggeri virali, alcuni di questi che hanno una lunghezza di 9 Kb portano l'informazione contenuta nei geni GAG e POL, questi messaggeri non vanno incontro a splicing e contengono esattamente l’intera formazione che era contenuta nel RNA genomico del virus infettante.
Abbiamo poi una seconda classe di RNA messaggeri che hanno un inferiore lunghezza, 4 Kb e questi messaggeri vanno incontro ad un unico processo di splicing, a seconda del punto in cui avviene lo splicing questa classe di messaggeri produce ENV, come pure vengono prodotti con questa modalità altre proteine che sono VPR, VIF e VPU.
Ultima classe ancora di dimensioni inferiori e che deriva dal messaggero che và incontro al ben 2 processi di splicing, questa classe comprende la proteina TAT,REV e NEF.
I ruoli di queste proteine nel ciclo di replicazione del HIV.
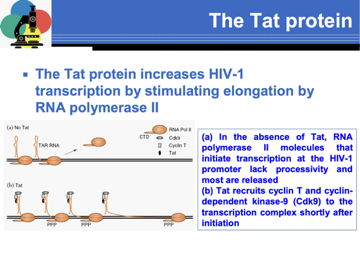
Un ruolo molto importante è svolto dalla proteina TAT, abbiamo un genoma virale integrato il quale deve trascrivere messaggeri, compito affidato all’RNA polimerasi 2, ma cosa succede se non è presente TAT?
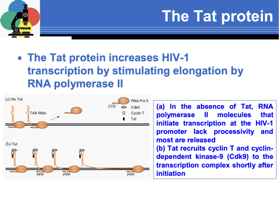
Qui abbiamo RNA virale integrato, la RNA polimerasi comincia a scorrere sullo stampo del pro virus, si forma un frammento di RNA virale che si ripiega a formare un forcina chiamata TAR= zona responsiva attack, ma poco dopo il processo di trascrizione si arresta e la RNA polimerasi 2 lascia lo stampo, cioè in assenza di TAT il processo di trascrizione sul pro virus è un processo abortivo. Se TAT è presente SLIDE vediamo ancora una volta lo stampo del pro virus, l'RNA polimerasi comincia il processo di trascrizione, l'RNA virale si ripiega a forcina ed ecco che TAT ha la possibilità di richiamare una chinasi ciclina dipendente (chinasi ciclina dipendente 9) la chinasi e la ciclina si legano alla forcina di RNA e questo determina che la chinasi vada a fosforilare l RNA polimerasi DNA dipendente cellulare. Una volta fosforilata ecco che la polimerasi acquista la capacità di formare dei messaggeri completi dell'intera formazione virale integrata. Quindi inizia la trascrizione in assenza di TAT ma subito dopo non c'è progressività nella trascrizione e RNA polimerasi DNA dipendente si dissocia, è necessaria la presenza di TAT per richiamare la chinasi ciclina dipendente e solo in questo caso per l avvenuta fosforilazione della RNA polimerasi il processo di trascrizione dell'intera formazione del pro virus può essere trascritto con conseguente formazione degli RNA messaggeri virali. Se TAT interviene nella trascrizione il ruolo di REV fondamentale è quello di consentire la traduzione degli RNA messaggeri virali. Abbiamo dei messaggeri virali che non vengono sottoposti a splicing e sono i messaggeri che portano l'informazione per GAG e POL, mentre altri messaggeri sottostanno ad un unico processo di splicing oppure a 2 processi di splicing. Solo la classe di RNA messaggeri di 2 Kb, messaggeri che portano alla sintesi di TAT, NEF, e REV, possono una volta sintetizzati lasciare il nucleo e portarsi nel citoplasma dove saranno tradotti nelle corrispondenti proteine. I messaggeri di maggiore dimensioni 4 e 9 Kb non sono in grado di lasciare il nucleo. In assenza di REV questi messaggeri vanno incontro nel nucleo a degradazione.
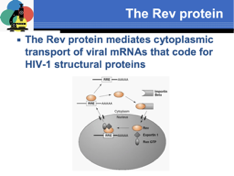
Il trasporto di questi messaggeri dal nucleo al citoplasma è possibile attraverso l'intervento di REV. REV ha un meccanismo d'azione del tutto sovrapponibile a quello della proteina REX. (Slide) della proteina REV libera nel citoplasma dove è stata appena sintetizzata grazie all'intervento dell'importina beta, REV riesce ad entrare nel nucleo dove si lega nei messaggeri di maggiori dimensioni a delle sequenze indicate come elementi responsivi a REV (SLIDE questo tratteggiato in verde che finisce con la coda di poli A è un messaggero non sottoposto a splicing o che è stato sottoposto a splicing una volta sola, quindi quelli di maggiori dimensioni, REV riconosce degli elementi responsivi a REV vi si lega assieme a l'esportina 1 e a Ran GTP e così realizza la possibilità che questi messaggeri dal nucleo possano migrare al citoplasma, dove il messaggero a contatto con i ribosomi viene liberato e REV rientra in circolo.
Quindi un ruolo determinante per far si che tutti i messaggeri virali possano raggiungere il citoplasma ed essere tradotti nelle corrispondenti proteine virali. Abbiamo poi tutta un'altra serie di proteine che nel corso della replicazione del HIV hanno un ruolo accessorio, cioè aiutano i virus a creare un ambiente che sia al massimo favorevole alla replicazione del virus, un esempio di questo ci viene proposto dalla proteina Nef
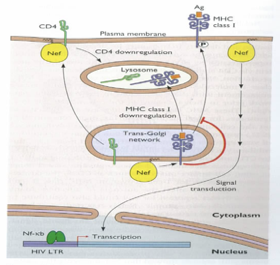
Nef deve il suo nome al fatto che agli inizi degli studi sul ciclo replicativo dell'HIV si riteneva che la proteina avesse un ruolo negativo nella replicazione. Oggi al contrario sappiamo che questa proteina interviene sulla cellula ospite agevolando la replicazione ed è anche un fattore importante della patogenicità dell'HIV. Cosa fa Nef? Alla superficie della cellula infettata dell'HIV sono presenti delle molecole di CD4, è proprio questo il recettore che riconosciuto dalla gp120 consente al virus di infettare la cellula, ed è anche un importante mediatore della risposta immunitaria. Compito di Nef è quello di allontanare dalla membrana citoplasmatica della cellula all'interno della quale l'HIV si sta replicando la proteina CD4 e lo fa in questa maniera: si lega Nef alla coda citoplasmatica di una molecola di CD4, interviene una proteina adattatrice, chiamata AP2, ed ecco che in una zona di membrana citoplasmatica rivestita di clatina, muovono le molecole di CD4, si forma una vescicola di endocitosi nella quale sono contenute le varie molecole di CD4 rimosse dalla superficie della cellula del linfocita, questa vescicola poi sarà portata a livello dei lisosomi, dove le molecole CD4 verranno degradate. C'è anche un'altra molecola a livello della superficie del linfocita che disturba l'HIV ed è la molecola MHC di classe I. Qual è il ruolo delle molecole del complesso maggiore di istocompatibilità? È quello a livello del RE dove arrivano i prodotti di degradazione dei prodotti virali, quindi antigeni, devono essere presentati alla superficie della cellula infettata per stimolare la risposta di altre cellule immunocompetenti. Lo vediamo qua, una proteina MHC di classe I che espone un antigene che è il prodotto di degradazione di una delle proteine dell'HIV. In questa maniera la cellula presenta l'antigene rendendosi riconoscibile da parte di cellule del sistema immunocompetente. Cosa ha pensato l'HIV? Lui vuole rimanere nascosto per avere tutto il tempo necessario per poter svolgere il suo ciclo replicativo. Il compito di Nef è arrestare il trasporto delle proteine MHC di classe I che portano legato l'antigene dal Golgi alla membrana citoplasmatica della cellula. Quindi prima funzione di Nef: rimozione di cellule CD4 e impedimento alle molecole MHC di classe I di raggiungere la membrana citoplasmatica del linfocita infetto. Ma non si limita qui l'intervento di Nef: essa è anche in grado di intervenire nella trasduzione del segnale, ha bisogno di fattori di trascrizione dalla cellula, vuole una cellula in attiva espressione l'HIV e il compito di Nef è quello di incrementare la trasmissione cellulare perché quella cellula sia in un momento di massima espressione, in altre parole l'HIV vuole a sua disposizione tutti i fattori di trascrizione che la cellula ha quando è in un momento di massima espressione.
Un altro effetto di Nef è quello di intervenire nella via di trasmissione del segnale ostacolando quei segnali che inducono apoptosi nella cellula. Il virus non vuole che la cellula vada in apoptosi perché non può andare avanti la sua replicazione. Ecco quindi che il ruolo di Nef è quello di bloccare l'apoptosi in modo che il virus abbia il tempo per realizzare e completare il proprio ciclo replicativo.
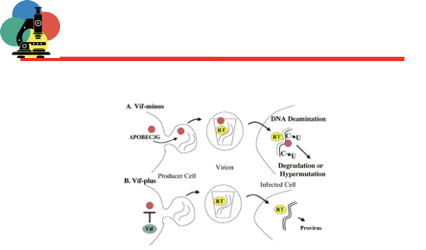
Un’altra proteina che interviene per salvare il virus da un attacco antivirale presente nella cellula è VIF. In assenza di VIF cosa succede?
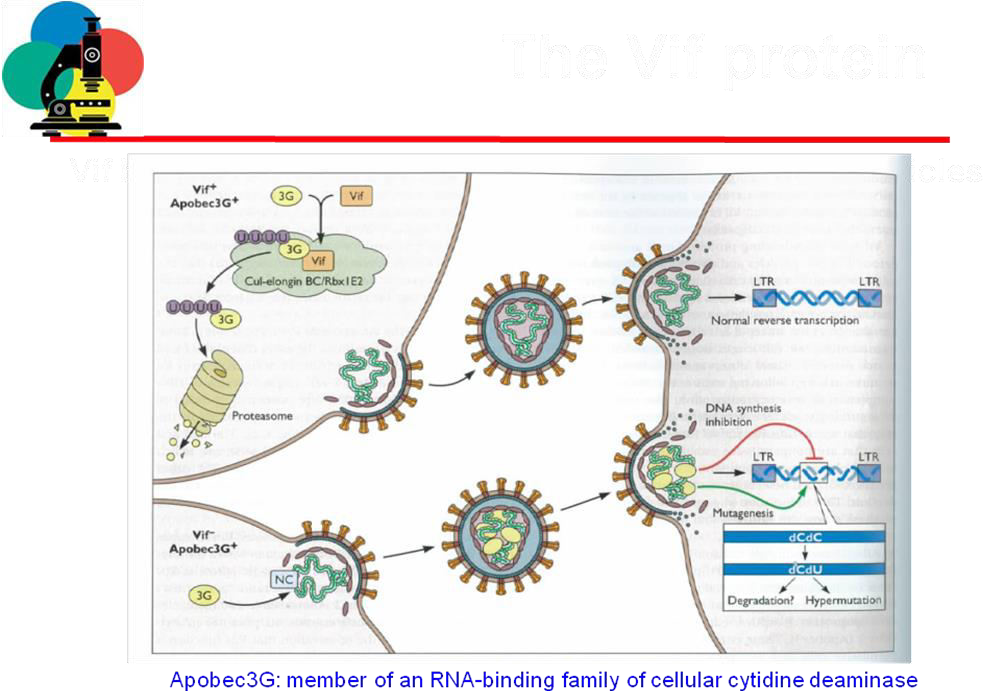
Qui abbiamo un momento terminale del ciclo replicativo di HIV quando a livello della membrana citoplasmatica dove sono state inserite la proteine GP41 e GP120, si sta assemblando una nuova particella virale che fuoriesce per gemmazione. C’è un pericolo a questo punto rappresentato da una proteina cellulare che ha attività antivirale, Apobec3G. È un enzima con attività di citidina o deossicitidina deamminasi. Se questa attività enzimatica entra quale componente di una particella virale apparentemente va tutto bene, il virus si impacchetta e ha la capacità di andare a infettare un’altra cellula.
Ma cosa succede quando va a infettare un’altra cellula?
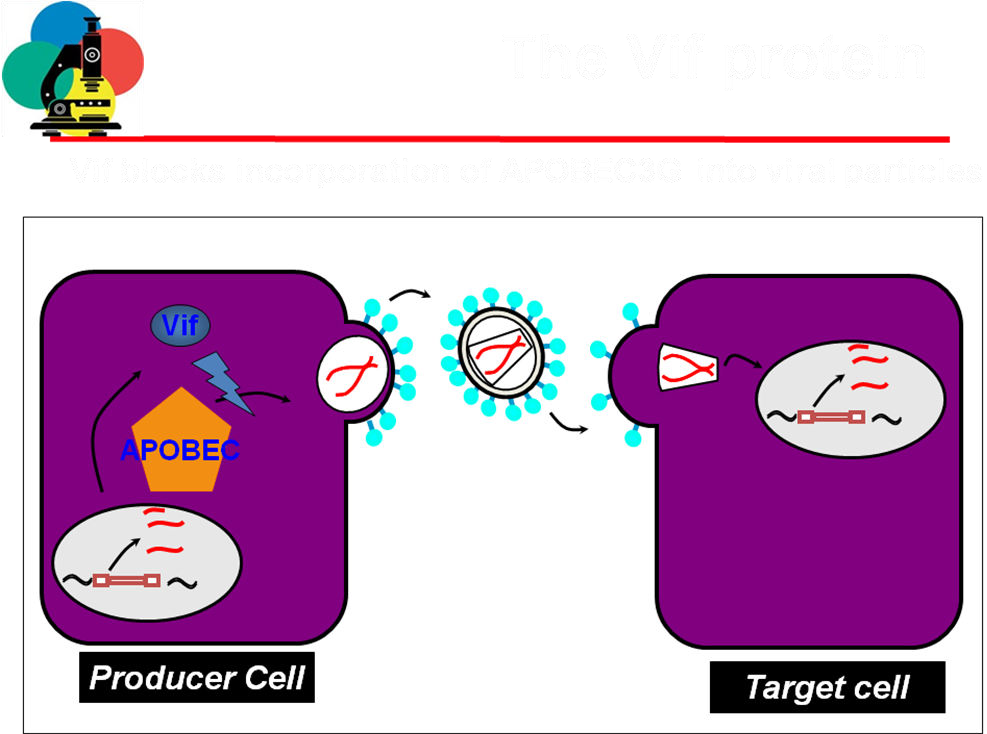
La prima espressione del virus nel citoplasma della cellula infettata è quella di realizzare il processo di trascrittasi inversa. Determina deamminazione nel corso della trascrittasi inversa della citidina in uracile ed ecco che il risultato del processo di trascrizione è un provirus stracarico di mutazioni e si può avere o ipermutazione oppure il risultato che al termine del processo di trascritasi inversa, questo DNA neosintetizzato venga degradato, quindi un enzima che provoca deamminazione del DNA che ha come punto finale l’insorgenza di varianti ipermutate che non possono andare incontro ad altri cicli replicativi oppure la degradazione diretta del provirus. Tutto questo all’HIV non piace, quindi ha evoluto una proteina che è Vif, capace di legare l’Apobec3G e una volta che l’ha legato determina dopo un ubiquitinizzazione, degradazione a livello dei ribosomi. Quindi contrasta una proteina che è dotata di potere antivirale presente nella cellula. Ecco qui un altro schema: questa è la cellula dove l’HIV si sta replicando, il virus è in una delle sue fasi finali del ciclo di replicazione, sta gemmando in quella porzione della membrana citoplasmatica dove sono state inserite la GP120 e GP41, c’è il pericolo che questo enzima in grado di deamminare il DNA nella successiva fase di retrotrascrizione quando questo virus andrà a infettare un’altra cellula bersaglio. VIF impedisce che questa attività enzimatica entri a far parte di una nuova particella virale, che essendo libera da questo fattore enzimatico potrà tranquillamente andare incontro ad un processo di trascritasi inversa una volta che avrà infettato un’altra cellula. Altra attività importante è quella svolta dalla proteina prodotta dal gene Vpr.
 Vpr
Vpr svolge un ruolo importante in quanto fa parte di quel processo di preintegrazione che dal citoplasma muove verso un poro nucleare in modo da consentire il passaggio del Provirus nel nucleo dove grazie all'integrasi potrà integrarsi. Quindi Vpr consente il passaggio del virus e lo fa con la collaborazione della proteina di matrice, quindi una funzione di trasporto dal citoplasma nel nucleo. Un'altra funzione di Vpr è quella di arrestare la cellula in G2. Perché lo fa? Quando la cellula è in G2 è al massimo la sua capacità di trascrivere messaggeri, tutti i fattori di trascrizione sono a disposizione per più lungo tempo e quindi è il momento dove realizza al meglio le proprie trascrizioni. Vpr si lega ad una fosfatasi, CDC25C. Qual è il suo ruolo fisiologico? Questo è un complesso di due proteine che partecipano all' arresto in G2. Per poterlo fare devono essere defosforilate e lo fanno grazie all'intervento di questa fosfatasi CDC25c. Questo è come vanno le cose in una cellula non infettata. Una volta che queste proteine sono defosforilate possono agire nel regolare la transizione del ciclo cellulare. Vpr si lega alla fosfatasi, impedisce che queste proteine vengano desfoforilate, di conseguenza non si avrà progressione del ciclo cellulare, ma la cellula rimarrà bloccata in G2. Recenti risultati indicano che c'è anche un terzo meccanismo d'azione di Vpr. Quando sta avvenendo nel complesso della retrotrascrizione, il processo di conversione del genoma da RNA a DNA, c'è il pericolo che residui di deossiuridina vengano incorporati nel DNA virale. Se questa situazione permane si avrà un tasso elevato di insorgenza di mutazioni. C'è un enzima cellulare che è una uracile-DNA glicosilasi che se impacchettata nel virione ha la possibilità di rimuovere i residui di deossiuridina incorporati e ristabilire il corretto appaiamento di basi. Il ruolo di VPR è quello di facilitare l'impacchettamento di questa attività enzimatica all'interno del virione in modo che eventuali errori commessi possano essere riparati.
Ultima proteina dell'HIV, tra quelle che intervengono sull'ambiente intracellulare per facilitare la replicazione di HIV, è Vpu.
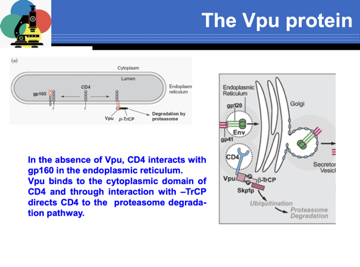
Ha una duplice attività. La prima: qui siamo nel RE di una cellula infettata da HIV. In questa sede troviamo sia le molecole GP120, ci sono molecole virali dal cui clivaggio deriveranno la GP120 e la GP41, come pure si trovano le molecole CD4 che la cellula ha sintetizzato che poi sono molecole che si sposteranno sulla sua superficie. Per il virus non è un incontro favorevole perché nel RE se GP120 e CD4 si legano insieme, la GP160 non avrà la possibilità di essere clivata in Gp120 e GP41 e raggiungere la membrana citoplasmatica di quella cellula. In altre parole il CD4 cellulare a livello del RE può bloccare la glicoproteina GP160 e questo non è gradito dal virus perché vuole che questa proteina glicoproteina GP160 sia clivata nei suoi due peptidi costituenti che verranno piazzati nella membrana citoplasmatica nei punti nel quale il virus gemmerà per formare una cellula virale completa e infettante. Ecco che nel RE il ruolo di Vpu è quello di legarsi con l'intervento di un'altra proteina cellulare al CD4 e ne determina la degradazione a livello dei proteosomi. Non si limita qui il ruolo di Vpu. C'è un'altra proteina appartenente alla famiglia delle deterine dalla quale l'HIV si deve difendere. Qui vediamo un virus che sta completando il suo processo di morfogenesi e sta gemmando da quella posizione di membrana citoplasmatica e linfocita dove sono state inserite la GP120 e GP41. C'è localizzata nella membrana citoplasmatica della cellula, molecole di questa proteina , della deterina, che hanno la tendenza a far si che legandosi alla particella virale questa sia di nuovo reinglobata nella cellula dove questo virus si era formato a una volta che è di nuovo ingerito nella cellula questa particella virale è destinata alla degradazione. Vpu si lega alla deterina facendo si che le particelle virali complete e infettanti di HIV possano liberarsi in ambiente extracellulare.
Siamo arrivati al provirus integrato, abbiamo visto come grazie all'intervento della RNA polimerasi II si riesce a sintetizzare diverse classi di mRNA e abbiamo visto come ci sono messaggeri che non vanno incontro a splicing, sono i messaggeri che portano l'informazione per gag e gag-pol. La maggior parte dei casi di questo processo di trascrizione, riconoscendo un segnale di terminazione, questi trascritti portano esclusivamente i trascritti di gag. Poi vi ricordate, ne abbiamo parlato nel discorso iniziale dei retrovirus ci può essere, grazie alla formazione di un ripiegamento a forcina, lo stallo dell'RNA polimerasi sullo stampo di DNA virale comporta un cambiamento del modulo di lettura che fa si che la tripletta segnale di stop non venga riconosciuta, in questo caso il processo di trascrizione va avanti e si viene a formare un messaggero più lungo che contiene sia l'informazione derivante da gag sia quella da pol. Così si forma un messaggero che tradotto darà luogo alla sintesi delle proteine enzimatiche proteasi, trascrittasi inversa e integrasi. I messaggeri più piccoli, nef e hanno possibilità una volta prodotti di lasciare il nucleo, mentre questi di maggiori dimensioni come pure quelli che derivano da un unico processo di splicing riescono a raggiungere il citoplasma con l'intervento di REP. Abbiamo sintetizzato, in altre parole, tutti i messaggeri che servono al virus di arrivare alla sintesi di tutte le sue proteine strutturali, regolatorie, accessorie indispensabili per il ciclo replicativo
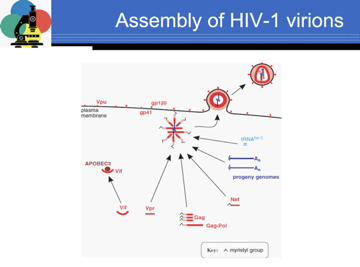
Qui abbiamo schematizzato un momento finale per il ciclo di replicazione e uno stadio di assemblaggio in cui due molecole di RNA genomico si portano dietro il transfer della lisina, vengono circondate da precursori delle proteine strutturali e queste proteine non sono però ancora funzionali. È un momento molto importante del virus, ed è grazie alle proteasi questi precursori polipeptidici durante la gemmazione e anche successivamente clivano i vari precursori polipeptidici per fornire il virus di tutte le corrette proteine che devono partecipare alla sua struttura. Dal clivaggio di gag si formeranno la proteina per la matrice, la proteina capsidica e quella nuclocapsidica, dal clivaggio di pol si formeranno le 3 attività enzimatiche presenti nel core dell'attività enzimatica. Qui vedete ricordato il ruolo di vif che è quello di impedire che l'attività deaminasica possa penetrare in una particella virale compromettendone il processo di retrotrascrizione quando questo virus infetta un'altra cellula.
Quindi abbiamo visto come l'HIV realizza la formazione di nuove particelle infettanti che liberate in ambiente esterno avranno la possibilità di infettare altre cellule.
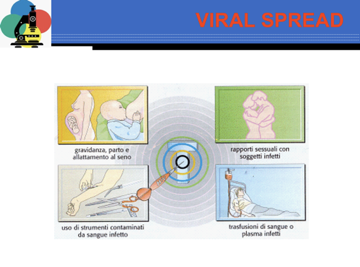
Per quanto riguarda le modalità di trasmissione: importante la trasmissione sessuale sia rapporti etero che omosessuali, trasfusione di sangue, plasma infetti, con strumenti contaminati da sangue e questo facilita la trasmissioni in individui che usano droghe. È possibile la trasmissione del virus dalla madre al feto in gravidanza o nel parto, o nell’allattamento perché il virus è presente nel latte materno.
La risposta immunitaria al virus dell'HIV
Come si difende il virus dall'ospite? La Retrotrascrizione è un'attività enzimatica estremamente inaccurata, ogni volta che viene prodotto un DNA provirus è possibile che la RetroTrascrittasi provochi da 1 a 10 mutazioni. Ecco che questo elevato tasso mutazionale fa si che le proteine di superficie del HIV abbiano un'enorme variabilità. Si formano anticorpi neutralizzanti nei quali la variabilità fa che queste proteine cambino, anticorpi precedentemente formati perdono la possibilità di essere anticorpi neutralizzanti, il nostro sistema immunocompetente deve di nuovo ripartire per realizzare una risposta umorale specifica contro le nuove varianti proteiche e questo serve al virus per sfuggire alla risposta immunitaria ed è anche il motivo che rende tutt'oggi estremamente difficile la realizzazione di un vaccino che renda impossibile l'insorgenza dell'AIDS. Sicuramente il colpo principale che l'HIV dà al nostro sistema immunocompetente è dove vanno a replicare? L'HIV replica in cellule dendritiche, in macrofagi, in linfociti CD4, che sono i principali attori di quella che è la risposta immunitaria. Mette in ginocchio con un attacco diretto il nostro sistema immunitario perché colpisce le cellule chiamate in causa per realizzare una risposta immunitaria.
Come vanno le cose in seguito all'infezione da HIV? Qui è avvenuta tramite ingresso di sangue infetto in un organismo di un individuo: nell'arco di tempo dalle 3 alle 6 settimane si sviluppa quella che noi chiamiamo infezione primaria. Può manifestarsi clinicamente, assomiglia per certi versi alla mononucleosi: febbre, dolori muscolari, possibilità che si manifesti un esantema. Nell'arco di breve tempo scompare.
Cos'è successo? Se andiamo a esaminare il sangue di questo soggetto vediamo che il picco di RNA di questo soggetto in circolo sale anche a valori molto elevati per poi diminuire grazie al nostro sistema immunocompetente. In concomitanza col picco che testimonia la replicazione del virus osserviamo un decremento del numero di linfociti CD4 che sono il bersaglio del virus. Questa infezione primaria guarisce apparentemente anche se vedete che il numero dei linfociti CD4 c'è una certa salita ma non raggiunge mai il valore iniziale. In un soggetto normale il numero dei linfociti è 1000/nL di sangue. C'è una certa risalita ma non si raggiungono i livelli di linfociti CD4 prima dell'infezione. A questo punto segue un lungo periodo di latenza. Apparentemente l'individuo è infettato dall'HIV, ma non manifesta alcuna sintomatologia clinica. È importante sottolineare che questa latenza clinica non corrisponde ad una latenza virologica. Alcuni distretti, in particolare nei linfociti di memoria, il virus è integrato, latente o non si esprime, ma nei linfonodi è attivo, ovvero si ha la continua produzione di nuove particelle di HIV.
Cosa avviene in questo periodo di latenza? Una sorta di lotta fra il sistema immunocompetente che cerca di contrastare l'infezione e il virus che lo attacca colpendo i linfociti e i macrofagi, i principali protagonisti della risposta immunitaria.
Il periodo di questa lotta, che in media si aggira intorno agli 8 anni, anche se in genere entrano in gioco fattori del virus o dell'ospite che influenzano questa lunghezza, dura sin tanto che il numero dei linfociti è mantenuto al di sopra di una soglia, quella di presenza di
200 linfociti per nL di sangue.
Il sistema immunocompetente è talmente compromesso che quest'ospite non riesce a contrastare l'infezione dei microrganismi che normalmente si comportano da opportunisti.
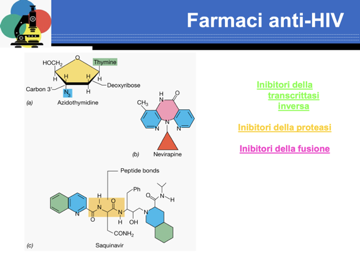
Come possiamo difenderci? Abbiamo a disposizione una serie di inibitori.
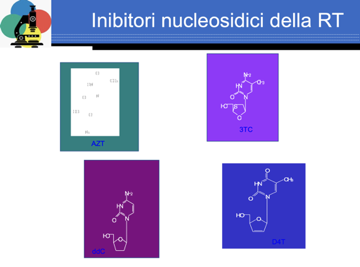
I primi ad essere stati scoperti sono stati gli inibitori della trascrittasi inversa, poi sono stati sviluppati quelli della proteasi, e oggi abbiamo a disposizione gli inibitori della fusione e della integrasi. Il primo inibitore scoperto è la azidotimidina.
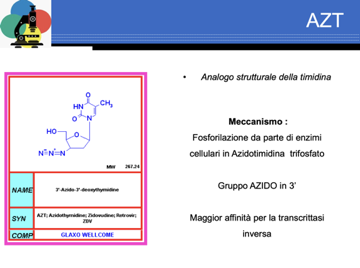
La molecola cosa ha di diverso rispetto alla timidina? In posizione 3' invece di presentare un gruppo –OH presenta un gruppo azide. Cosa succede quando l'azidotimidina penetra all'interno di una cellula dove l'HIV sta replicando? Succede che l'azidotimidina viene, da parte di enzimi cellulari, metabolizzata e convertita in azitimidina trifosfato. È un analogo della timidina che ha un gruppo azide in posizione 3' e la trascrittasi inversa (oramai vi ho detto tante volte che gli enzimi virali sono molto inaccurati) non riesce a distinguere l'azidotimidina trifosfato dalla timidina trifosfato e quindi la incorpora nel DNA provirus. Cosa determina l'incorporazione dell'azidotimidina nel provirus? Si comporterà da terminatore di catena, ma il gruppo -OH in posizione 3' è indispensabile per l'allungamento di una catena di DNA ed ecco che la sintesi del provirus verrà ad essere bloccata. Perché è selettivo? Mentre la RT (trascrittasi inversa) si fa ingannare e non distingue la timidina trifosfato e azidotimidina trifosfato, la DNA polimerasi della cellula, che lavora in maniera molto più accurata non incorpora l'azidotimidina trifosfato. Stiamo sintetizzando un provirus (slide), questo è un RNA genomico, G ha chiamato C, dovrebbe entrare perché c'è T.
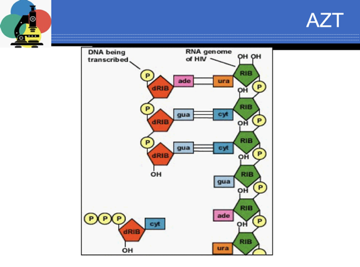
L'enzima fa confusione: anziché una timidina trifosfato prende un azidotimidina trifosfato e l'accoppia con A. Manca l'ossidrile in posizione OH. Qual è il risultato? Il risultato è che la sintesi del provirus viene bloccata. Con meccanismo simile agiscono molte altre molecole che abbiamo a disposizione.
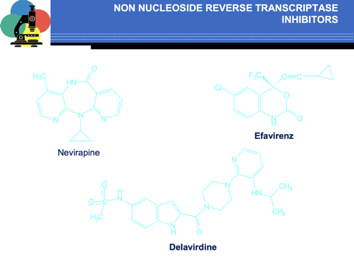
Tutte le molecole attivate dalla cellula nella forma trifosfato, fungono da terminatori di catena perché mancano del gruppo - OH in posizione 3'. Sono chiamati inibitori nucleosidici quelli che abbiamo analizzato adesso, perché sono analoghi di nucleosidi fisiologici, l'azidotimidina è un analogo della timidina. Un'altra classe di inibitori sono quelli non nucleosidici, caratterizzati dalle più svariate strutture chimiche, intervengono sulla RT.
Mentre gli inibitori nucleosidici si legano nel sito attivo della RT, gli inibitori non nucleosidici si legano in un sito adiacente della RT bloccandone la funzione. Hanno quindi un diverso meccanismo d'azione rispetto ai nucleosidici. Un esempio di inibitore non nucleosidico è la nevirapina.
Altre due classi di inibitori: inibitori della proteasi, che è l'attività enzimatica virale in fase di maturazione. Il compito qual'era? Si erano sintetizzano dei polipeptidi, la proteasi può clivare così si possono avere tutte le proteine virali sia quelle strutturali che enzimatiche nel momento di morfogenesi di una particella di HIV. Come funzionano? Questo è il precursore gag pol. Arriva la proteasi e la cliva in tutti i suoi costituenti: la matrice, la proteina capsidica, la proteina nucleocapsidica. Cosa avviene invece se è presente un inibitore della proteasi? Imitano la catena proteica che si inserisce nel sito attivo dell'enzima. Vi si legano ed ecco che rimangono agganciati. In altre parole sequestrano la proteasi, vi si legano, entrano in competizione con quello che è il substrato fisiologico, rimangono agganciati non permettendo che il precursore virale possa essere clivato generando le proteine virali. Un concetto importante è che tutti questi farmaci usati in terapia sono fallimentari per l'elevato tasso mutazionale.
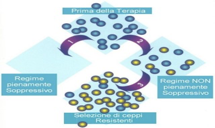
Si ha avuto un successo nella terapia? Utilizzando farmaci in associazione, colpiamo il virus utilizzando farmaci con diverso meccanismo d'azione in maniera tale da riuscire ad ostacolare la selezione di mutanti farmacoresistenti. Abbiamo a disposizione oggi varie combinazioni, è frequente la combinazione di 3 farmaci che impiega due inibitori della RT in associazione con un inibitore delle proteasi. E questo regime permette di portare a zero la quantità di HIV in circolo.
È importante perché? Questi sono virus in circolazione del sangue prima della terapia.
Se io ho una terapia che parzialmente sopprime la replicazione del virus, quindi il virus continua a replicare, facilito l'insorgenza di mutanti resistenti. Quand'è che questi mutanti non potranno emergere? Quando avrò un regime totalmente soppressivo, non c'è niente da selezionare. In associazione con i farmaci si riesce a portare a zero la quantità di HIV nel sangue.
Ci sono dei limiti, innanzitutto gli effetti tossici ed inoltre la terapia non può essere interrotta. Il virus instaura latenza, è molto importante lo stadio di latenza all'interno dei linfociti memoria: se uno sospende la terapia il virus integrato può riattivarsi e riprendere l'infezione. I farmaci sono in grado di controllare la replicazione dei virus, ma sono una terapia, non una cura e come il farmaco è soppresso, il virus dai punti dove si è nascosto può riprendere il proprio ciclo replicativo.
Altro aspetto negativo: sono farmaci, dal punto di vista brevettuale, con un costo elevato, per motivi economici la terapia è disponibile nei Paesi a maggior sviluppo economico-sociale, mentre non si hanno ancora interventi terapici nelle zone maggiormente colpite come l'Africa.
Qui (animazione slide) abbiamo il ciclo dell'HIV dall'inizio alla fine. Ecco l'interazione tra GP120 e Cd4, cambio conformazionale e si lega col recettore, seguirà l'esposizione di gp41 che consente all'envelope virale di fondersi con la membrana citoplasmatica della cellula. Il core virale è liberato nel citoplasma. Segue il processo di RT. Ecco la RT che su stampo di RNA monocatenario copia, prima fa una catena completa di DNA e nel frattempo distrugge l'RNA, scatta poi la funzione di DNA polimerasi DNA dipendente e arriviamo ad un DNA bicatenario che passa in un poro nucleare e grazie all'integrasi andrà a inserirsi nel genoma della cellula ospite. Grazie all'intervento della RNA polimerasi II il provirus può essere trascritto, questi azzurri che si stanno formando sono i messaggeri virali. Dovranno lasciare il nucleo ovviamente. Rev consente il trasporto dei messaggeri che non sono stati sottoposti a splicing, oppure sottoposti ad un unico splicing, e grazie a rev raggiungono i ribosomi nel citoplasma. Qui abbiamo la formazione del prodotto gag pol sotto forma di poliproteina, in maggior quantità viene prodotta gag. Queste poliproteine saranno tagliate alla fine dalle proteasi. Qui abbiamo invece la formazione delle poliproteine di superficie GP120 e GP41, formate sottoforma di un precursore che nel Golgi è una proteasi cellulare, le taglia in 2 e migrano alla superficie della cellula. Processo di morfogenesi. Le varie poliproteine con le due molecole di RNA genomico e il transfer partecipano ad un processo assemblaggio. È in questo stadio finale che la proteasi cliva le varie poliproteine formando le proteine strutturali e enzimatiche che concorrono alla formazione di una particella completa di HIV.