Classificazione dei monosaccaridi
I monosaccaridi o zuccheri semplici sono derivati aldeidici o chetonici di alcoli poliossidrilici a catena aperta con almeno tre atomi di carbonio.
Questi vengono classificati in base al loro gruppo carbonilico e al numero dei loro atomi di carbonio. Se il gruppo carbonilico è un aldeide, come nel glucosio, lo zucchero viene detto aldosio. Se, invece, il gruppo carbonilico è un chetone, come nel ribulosio, lo zucchero viene definito chetosio. I più piccoli monosaccaridi, quelli a tre atomi di carbonio, sono detti triosi. Quelli con quattro, cinque, sei, sette e così via, atomi di carbonio sono rispettivamente tetrosi, pentosi, esosi, eptosi, eccetera. Questi termini possono essere combinati e quindi il glucosio, per esempio, diventa un aldoesosio, mentre il ribulosio è un chetopentosio.
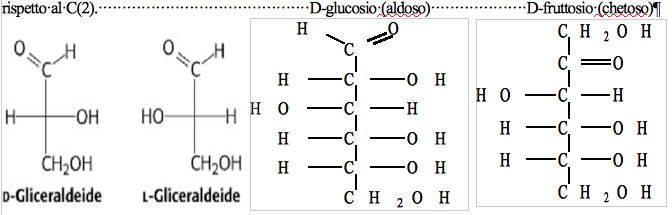
Un esame della formula chimica del D-glucosio rileva che tutti e sei i suoi atomi di carbonio, meno due, il C(1) e il C(6), sono centri chirali e di conseguenza il D-glucosio è uno dei 24=16 stereoisomeri che comprendono tutti i possibili aldoesosi. In generale gli aldosi, con n-atomi di carbonio hanno 2n-2 stereoisomeri. Emil Fischer, nel 1896, determinò la configurazione degli aldoesosi. In base alla sua convenzione, gli zuccheri D hanno la stessa configurazione assoluta della D-gliceraldeide a livello del centro asimmetrico più lontano dal loro gruppo carbonilico. Gli zuccheri L, sempre in base alla convenzione di Fischer, sono immagini speculari delle forme D. Gli zuccheri, invece, che differiscono soltanto per la configurazione intorno ad un atomo di carbonio vengono definiti epimeri l'uno dell'altro. Ad esempio il D-glucosio e il D-mannosio sono epimeri
CONFIGURAZIONI E CONFORMAZIONI
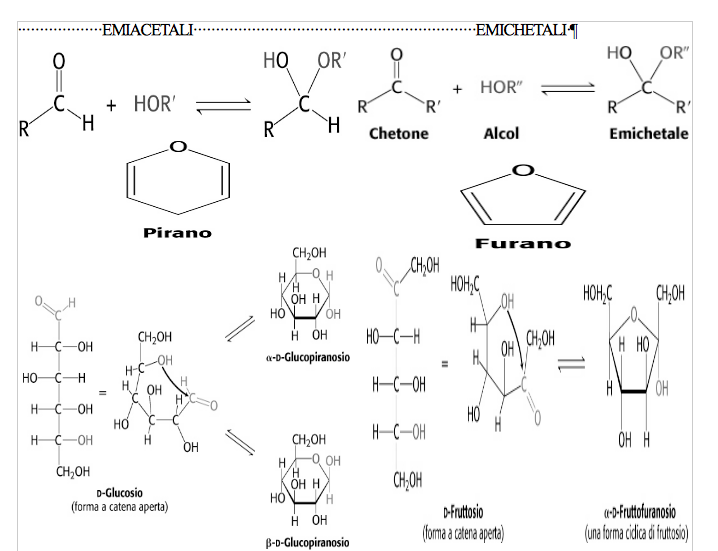
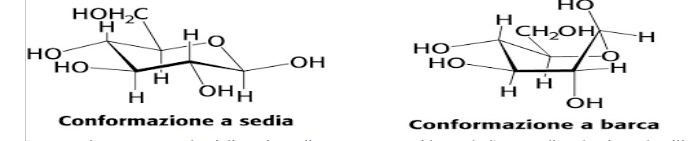
In generale, comunque, la ciclizzazione di un monosaccaride rende l'atomo di carbonio carbonilico asimmetrico. La coppia di diasteroisomeri che ne deriva vengono detti anomeri e l'atomo di carbonio emiacetalico o emichetalico diventa il carbonio anomerico. Nell'anomero α, il sostituente OH sul carbonio anomerico è sul lato opposto dell'anello saccaridico rispetto al gruppo CH2OH sul centro chiralico che definisce la configurazione D o L (il C5 negli esosi). L'altro anomero viene indicato con la lettera β. I due anomeri del D-glucosio, come ogni coppia di diasteroisomeri, hanno proprietà fisico e chimiche diverse. Per esempio, i valori del potere rotatorio specifico, per l'α-D-glucosio e per il β-D-glucosio sono rispettivamente +112,2° e +18,7°. Quando queste due sostanze pure sono disciolte in acqua, il potere rotatorio specifico si modifica lentamente fino a che non raggiunge il valore di +57,7°. Questo fenomeno è noto con il nome di mutorotazione; per il glucosio, essa deriva dalla formazione di una miscela in equilibrio costituita dal 63,6% dell'anomero β e dal 36,4% dell'anomero α. Come ben si può capire, quindi, la chimica degli zuccheri è in gran parte quella dei loro gruppi ossidrilici e carbonilici. Per esempio, in una reazione catalizzata da un acido, il gruppo ossidrilico anomerico di uno zucchero si condensa reversibilmente con gli alcoli per formare α- e β-glicosidi. Il legame che collega il carbonio anomerico e l'ossigeno acetalico viene detto legame glicosidico. I polisaccaridi sono tenuti insieme da questo legame tra le unità monosaccaridiche vicine.
Continua a leggere:
- Successivo: Classificazione dei polisaccaridi
- Precedente: Definizione di carboidrati
Dettagli appunto:
- Autore: Domenico Azarnia Tehran
- Università: Università degli Studi di Roma La Sapienza
- Facoltà: Scienze Matematiche, Fisiche e Naturali
- Corso: Scienze Biologiche
- Esame: Chimica biologica
- Titolo del libro: Biochimica
- Autore del libro: Donald Voet e Judith G. Voet
- Editore: Zanichelli
- Anno pubblicazione: 1993
Altri appunti correlati:
- Fisiologia della nutrizione
- Biologia molecolare
- Biochimica
- Struttura molecolare delle proteine
- Scienze e tecniche dietetiche applicate
Per approfondire questo argomento, consulta le Tesi:
- Crescita di Chlorella vulgaris in acque reflue da vinificazione: studio della cinetica di crescita e del contenuto in lipidi
- Evidenze nutrizionali per il recupero muscolare nell'atleta di endurance
- The role of CARMA2/CARD14 in NF-kB activation signalling
- Caratterizzazione delle specie ittiche di basso valore commerciale del Golfo di Manfredonia
- Approcci Sistemici e Transdisciplinari per la Gestione a lungo termine del Sovrappeso e dell’Obesità
Puoi scaricare gratuitamente questo riassunto in versione integrale.

