Collageni
Collageni
Eliche stirate in stereoforma d.
Presenza di amminoacidi destabilizzanti (G, P, O-Pro) per circa il 50%.
Periodo di 28 Ǻ, e il periodo proiettato sull’asse di avvolgimento comprende 10 aa (all’incirca il doppio di 1 α-elica).
L’angolo tra il piano perpendicolare all’elica e quello perpendicolare alla spira è maggiore di 30° (non c’è autostabilizzazione).
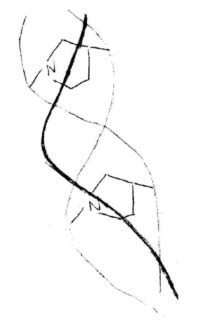
Stabilizzazione con interazioni di componenti diversi della proteina: organizzazione a eliche multiple (complessi di tre eliche).
Quando si formano sono tenute assieme da molecole saccaridiche (nelle posizioni 1, n, centrale). Reagiscono con i residui amminoacidici, e si distribuiscono lungo tutta la lunghezza dell’elica tripla.
INVECCHIAMENTO
Quando il collagene invecchia, le interazioni con i saccaridi si perdono. Compaiono nuove interazioni grazie alla lisina.
A-CH2-NH2 → A-CHO + NH3 DEAMMINAZIONE OSSIDATIVA
Residui di lisina modificati possono reagire con i residui di lisina non modificati, se affacciati.
A-CH2 + A-CHO (ATTACCO NUCLEOFILO)
Si forma con legame covalente da un’elica all’altra.
Il sistema diventa più compatto, e la solubilità diminuisce.
Le unità a 28 Ǻ (10 aa) si ripetono nei sistemi modificati per lunghezze di 10 aa: macroperiodi di 2800 Ǻ.
Continua a leggere:
- Successivo: Struttura terziaria
- Precedente: Proteine fibrose
Puoi scaricare gratuitamente questo appunto in versione integrale.

