Glucosidasi
Scindono legami glicosidici.
Sono endoglicosidici ed esoglicosidici.
Discriminano tra legame α e β-glucosidico.
Le amilasi sono per polisaccaridi ramificati, riconoscendo i punti da idrolizzare in base alla gerarchia strutturale.
Vanno avanti fino all’esaurimento producendo oligosaccaridi a 3 o 4 elementi, o riescono a degradare fino al maltoso.
Operano per protonazione/deprotonazione.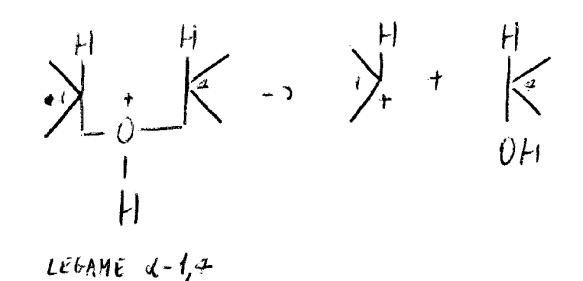
Alcune si sono evolute come metallo-enzimi, con un aumento della velocità di catalisi.
Le endoglicosidasi agiscono sul legame α dando effetti che continuano perché i punti di idrolisi vengono riconosciuti in virtù delle gerarchie strutturali.
POLISACCARIDI → DESTRINE → OLIGOSACCARIDI → DISACCARIDI (DIGESTIONE ESAURIENTE)
Si ottiene il maltoso (legame α-1,4) proveniente dalla catena lineare, e l’isomaltoso (legame α-1,6) proveniente dalle ramificazioni.
Se ci sono polisaccaridi lineari (amiloso) agiscono le esoamilasi (β-amilasi) che agiscono sempre sul legame α. Gli enzimi riconoscono le catene lineari nel terminale non riducente. Il sito catalitico è abbastanza profondo da accettare due residui glicosidici (due unità saccaridiche). Il secondo legame glicosidico si trova di fronte a un residuo di istidina per la protonazione. Partendo dall’estremo riducente viene staccata un’unità di maltoso per volta.
Meccanismo simile per le β-glicosidasi, che scindono legami β-glicosidici: si inidrizzano verso la cellulosa (cellulasi), la emicellulosa (emicellulasi) o i mucopolisaccaridi (mucopolisaccarasi).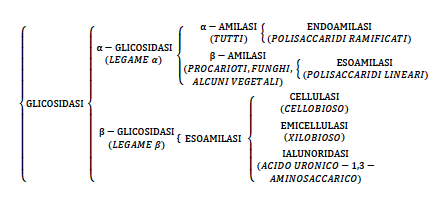
I polisaccaridi β sono a lunga vita: infatti solo gli esoenzimi (β-glicosidici) li attaccano, con velocità molto bassa, e solo quando le strutture sono già disorganizzate.
Continua a leggere:
Dettagli appunto:
-
Autore:
Marco Lazzara
[Visita la sua tesi: "Determinazione di arsenico mediante voltammetria di stripping anodico con elettrodo in oro"]
[Visita la sua tesi: "I laser a coloranti: fondamenti e stato dell'arte"]
- Università: Università degli Studi di Torino
- Facoltà: Scienze Matematiche, Fisiche e Naturali
- Corso: Chimica
- Esame: Biochimica
- Docente: Carlo Giunta
Altri appunti correlati:
- Biochimica
- Fondamenti di chimica
- Appunti di Biochimica
- Catecolamine e glucagone
- Chimica Analitica Strumentale (Spettroscopia)
Per approfondire questo argomento, consulta le Tesi:
- Analisi dei nitriti attraverso il loro impiego nell’industria alimentare e applicazione di un’indagine percettiva sui consumatori
- Meccanismi biochimici ed effetti sulla salute umana del licopene
- Studio dei processi di degrado su manufatti archeologici in ambiente marino sommerso e sperimentazione di procedure innovative per la conservazione in situ
- Bio-lubricant from the olive mill waste through a new biocatalyst immobilized on ZnFe2O4
- Rational Design and Synthesis of Novel Acadesine-Like Modulators of AMPK
Puoi scaricare gratuitamente questo appunto in versione integrale.

